Tous les sujets
Tous les sujets Maths
Maths Physique-Chimie
Physique-Chimie Corrigés de BAC
Corrigés de BAC Révisions Maths lycée
Révisions Maths lycée Prépa Examens
Prépa Examens
 Tous les sujets
Tous les sujets Maths
Maths Physique-Chimie
Physique-Chimie Corrigés de BAC
Corrigés de BAC Révisions Maths lycée
Révisions Maths lycée Prépa Examens
Prépa Examens
Autour du manganèse
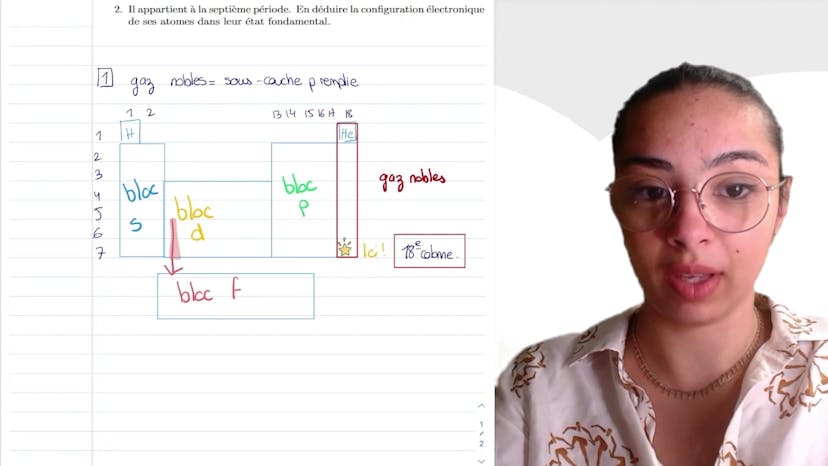
Le cours porte sur le manganèse et aborde les sujets des configurations électroniques, des énergies de ionisation et de la classification périodique. La structure électronique fondamentale de l'atome de manganèse est 1s², 2s², 2p6, 3s², 3p6, 4s² et 3d5. L'élément appartient au bloc D de la classification périodique en raison de la sous-couche D en cours de remplissage. Les degrés d'oxydation accessibles au manganèse sont de 1 à 7, car il a 7 électrons de valence. Les degrés d'oxydation les plus stables pour le manganèse sont +2 et +7. Les énergies de troisième ionisation de certains éléments de la période du manganèse sont discutées, avec un écart particulièrement élevé pour le fer en raison de sa sous-couche D semi-remplie. Il est également souligné que lors de la formation d'ions, les électrons sont enlevés dans l'ordre croissant des niveaux d'énergie.